
Dulong-Petit-Gesetz
Das Dulong-Petit-Gesetz (nach Pierre Louis Dulong und Alexis Thérèse Petit) besagt, dass die molare Wärmekapazität eines aus einzelnen Atomen zusammengesetzten Festkörpers einen universalen und konstanten Wert habe, nämlich das Dreifache der universellen Gaskonstante R:
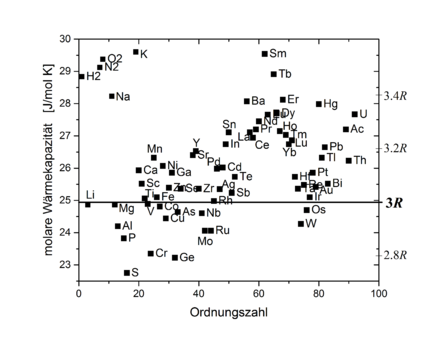
Die beiden Namensgeber stellten experimentell fest, dass zahlreiche von ihnen
untersuchte Substanzen
praktisch dieselbe molare Wärmekapazität haben, und veröffentlichten 1819 die
Vermutung, es handle sich hierbei um eine allgemeine Gesetzmäßigkeit. Die
klassische statistische
Thermodynamik (die noch keine Quanteneffekte
kannte), fand später für die molare Wärmekapazität monoatomarer (das heißt aus
gleichartigen Atomen aufgebauter) Festkörper tatsächlich den konstanten Wert
.
Auf größere Temperaturbereiche
ausgedehnte Messungen und theoretische Untersuchungen unter Berücksichtigung
quantenmechanischer Prinzipien zeigen jedoch, dass dieses Gesetz nur näherungsweise
gültig ist.
Herleitung
Die Teilchen in einem Festkörper
sind an ihre Plätze im Kristallgitter
gebunden und führen Schwingungen
um diese Mittelpositionen
aus. Die Schwingung jedes Teilchens kann in erster Näherung als harmonischer
Oszillator beschrieben werden. Nach dem Gleichverteilungssatz
der klassischen statistischen Thermodynamik trägt jeder der drei Gitterschwingungsfreiheitsgrade jedes
Teilchens (je einer in -,
-
und
-Richtung)
bei der Temperatur
im Mittel die kinetische
Energie
mit der Boltzmannkonstante
.
Die potentielle Energie des harmonischen Oszillators ist eine homogene Funktion 2. Grades in der Auslenkung. Also folgt nach dem Virialsatz, dass die mittlere potentielle Energie gleich der mittleren kinetischen Energie ist:
Auf einen Schwingungsfreiheitsgrad entfällt daher im Mittel die Energie
und auf ein Teilchen mit drei Freiheitsgraden für die Gitterschwingung die
Energie
.
Ein Mol solcher
Teilchen trägt also die Energie
mit
und die molare Wärmekapazität ist
mit
die Stoffmenge
die molare Wärmekapazität bei konstantem Druck
die molare Wärmekapazität bei konstantem Volumen
die molare innere Energie
die molare Enthalpie.
Grenzen
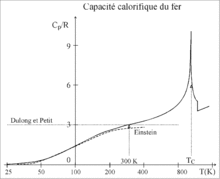
Trotz seiner Einfachheit macht das Dulong-Petit-Gesetz relativ gute Voraussagen für die spezifische Wärmekapazität von Feststoffen mit einfacher Kristallstruktur bei hinreichend hohen Temperaturen (z.B. bei Raumtemperatur).
In Bereichen niedriger Temperaturen weicht es zunehmend von den
experimentellen Befunden ab. Da die Gitterschwingungen quantisiert
sind, können sie pro Freiheitsgrad nur Energiequanten der Größe
aufnehmen (
Plancksches
Wirkungsquantum,
Schwingungsfrequenz). Insbesondere ist
mindestens die Energie
pro Freiheitsgrad nötig, um die Schwingung überhaupt anzuregen. Ist die zur
Verfügung stehende thermische
Energie
zu gering, so werden einige Freiheitsgrade gar nicht angeregt und können nicht
durch Energieaufnahme zur Wärmekapazität beitragen. Die Wärmekapazität von
Festkörpern nimmt daher bei sehr niedrigen Temperaturen merklich ab und strebt
für
gegen Null (Dritter Hauptsatz der Thermodynamik).
Hier liefert das Debye-Modell
bessere Voraussagen.
Ist ein Festkörper nicht aus einzelnen Atomen, sondern aus komplizierteren Molekülen aufgebaut (z.B. CaSO4), so kommen zu den 3 Freiheitsgraden der Gitterschwingung für jedes Teilchen zusätzliche Freiheitsgrade der Molekülschwingung hinzu (die Teilchen des Moleküls schwingen gegeneinander). Die molare Wärmekapazität eines solchen Festkörpers kann deutlich höher sein als vom Dulong-Petit-Gesetz vorhergesagt.
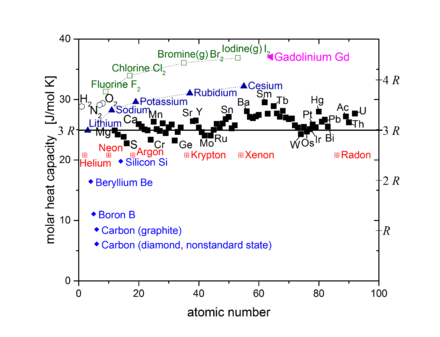
Metalle
als monoatomare Festkörper befinden sich meist in guter Übereinstimmung mit dem
Dulong-Petit-Gesetz. Wegen der Metallbindung würde man
zunächst anderes erwarten, da die Atome bei ihrer Bindung Elektronen aus ihrer äußeren
Elektronenhülle
abgeben, welche sich frei durch den Kristall bewegen können (Elektronengas). Jedes
Elektron müsste 3 Translationsfreiheitsgrade
beitragen, so dass, wenn jedes Atom ein Elektron abgibt, die molare
Wärmekapazität
betragen müsste. Da im Elektronengas aber bereits alle Zustände
unterhalb der Fermi-Verteilung
besetzt sind, können die meisten Elektronen nicht in einen Zustand höherer
Energie übergehen und daher auch nicht zur Wärmekapazität beitragen.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 28.06. 2024