Heteroaromaten
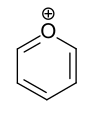
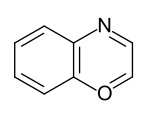
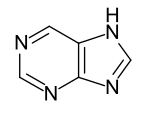
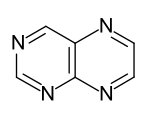
Bei den Heteroaromaten handelt es sich um aromatische Verbindungen, deren Ringgerüst ein oder mehrere Heteroatome (z. B. Stickstoff, Sauerstoff, Schwefel) enthalten. Formal leiten sich Fünf- und Sechsring-Heteroaromaten vom Cyclopentadienyl-Anion und vom Benzol ab, indem eine Ring-CH-Gruppe (Methingruppe) durch ein Heteroatom ersetzt wird.
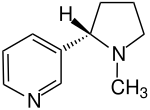
-one_200.svg.png)
Die Heteroaromaten spielen eine bedeutende Rolle in der Naturstoffchemie (Beispiele: Nikotin, Coffein) und in der Pharmazie. So handelt es sich bei Antipyrin, dem ersten synthetischen fiebersenkenden Arzneimittel (1887) um einen Fünfring-Heteroaromat.
Eigenschaften
Monocyclische Heteroaromaten sind durch ein dem Benzol
analoges -Elektronensextett
(siehe Hückel-Regel)
gekennzeichnet.
Sie werden in
-elektronenreiche
und
-elektronenarme
Heteroaromaten unterteilt.
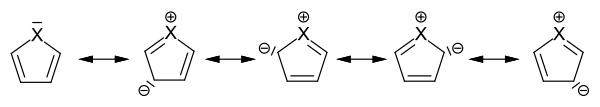
Bei den Fünfring-Heteroaromaten ist das nichtbindende freie Elektronenpaar Teil
des
-Elektronensextetts,
das sich im Sinne der mesomeren
Grenzstrukturen auf die fünf Ringatome verteilt.
Mesomere Grenzstrukturen bei Fünfring-Heteroaromaten
Dadurch erhöht sich auf Kosten des Heteroatoms die -Elektronendichte
an den Ring-Kohlenstoffatomen, so dass die Fünfring-Heteroaromaten zu den
-elektronenreichen
Heteroaromaten gehören.
Die -elektronenreichen
Heteroaromaten sind erwartungsgemäß reaktiver als die Aromaten ohne Heteroatom.
Die Reaktivität sinkt aber mit steigender Gruppennummer und Periode des
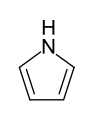
Heteroatoms. So neigt z.B. Pyrrol
zur Autopolymerisation,
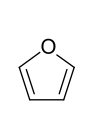
während Furan
unter Lufteinwirkung schnell braune Oxide
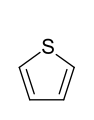
bildet, die sich thermisch wieder spalten lassen. Thiophen
hingegen ist an der Luft bereits recht beständig. Die typische Reaktion der drei
Verbindungen ist die elektrophile
Substitution. Nur Furan, der Heterocyclus mit der geringsten
Resonanzenergie, zeigt auch typische Reaktionen eines Diens.
Zusätzliche Heteroatome beeinflussen die Stabilität in Abhängigkeit von ihrer
Position im Ring. Beispielsweise führt ein Stickstoffatom in 3-Position generell
zu einer chemischen Stabilisierung eines
-elektronenreichen
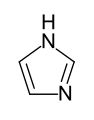
Heteroaromaten (siehe vglw. Imidazol,
Thiazol).
Bei den Sechsring-Heteroaromaten handelt es sich um -elektronenarme
Heteroaromate. So reagiert der Sechsring-Heteroaromat Pyridin nur noch unter
drastischen Bedingungen im Sinne einer elektrophile Substitution, jedoch sind
recht leicht nucleophile
Substitutionsreaktionen in 2- und 4- Stellung möglich.
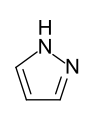
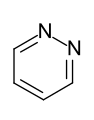
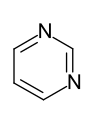
Fünfgliedrige Heterocyclen mit zwei Heteroatomen wie die 1,2-Diazole (Pyrazole) und die
1,3-Diazole (Imidazole) sind gegenüber dem schwach basischen Pyrrol stärkere
Basen, da sie ein weiteres Ring-Stickstoffatom enthalten, dessen freies
Elektronenpaar senkrecht zum -System
steht und das sich deshalb kaum an der Mesomerie beteiligt.
Typische Vertreter
Monocyclische Heteroaromaten
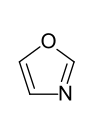
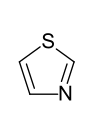
- Fünfring-Heteroaromaten mit einem Heteroatom:
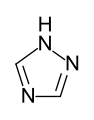
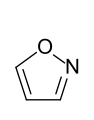
- Fünfring-Heteroaromaten mit mehreren Heteroatomen:
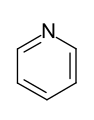
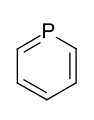
- Sechsring-Heteroaromaten mit einem Heteroatom:
benzol
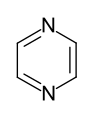
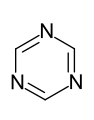
- Sechsring-Heteroaromaten mit mehreren Heteroatomen:
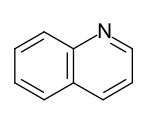
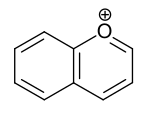
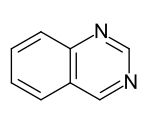
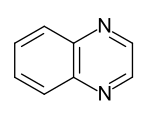
Bicyclische Heteroaromaten
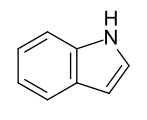
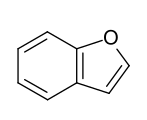
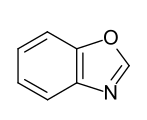
- Benzoanellierte Fünfring-Heteroaromaten:
- Benzoanellierte Sechsring-Heteroaromaten:
- Heteroanellierte Heteroaromaten
Siehe auch


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 28.11. 2024