
Pepsin
| Pepsin 3A | ||
|---|---|---|
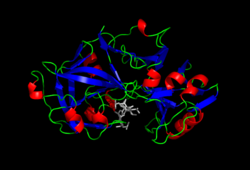
| ||
| Pepsin gehemmt durch Pepstatin | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 326 bzw. 332 Aminosäuren | |
| Präkursor | Pepsinogen, 373 AS | |
| Bezeichner | ||
| Gen-Name |
| |
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code |
| |
| Enzymklassifikation | ||
| EC, Kategorie | ||
| MEROPS | ||
| Reaktionsart | Hydrolyse (Proteolyse) | |
| Substrat | Proteine | |
| Produkte | Peptide | |
| Vorkommen | ||
| Homologie-Familie | Aspartin Endopeptidase | |
| Übergeordnetes Taxon | Eukaryoten | |
Pepsin (von altgriechisch πέψις pepsis, „Verdauung“) ist ein Verdauungsenzym, eine so genannte Peptidase, die in den Hauptzellen des Magenfundus von Wirbeltieren und somit auch dem Menschen gebildet wird. Sie ist für den Abbau von mit der Nahrung aufgenommenen Eiweißen (Proteinen) zuständig. Als Inhaltsstoff in Nahrungsmitteln oder in Pepsinwein soll es die Verdauung fördern.
Geschichte
Grundlage für den Versuch von Johann Nepomuk Eberle im Jahr 1834 Pepsin aus Rindermägen anzureichern und somit zu beweisen, dass die Eiweißverdauung ein chemischer Prozess ist, waren die Aufzeichnungen von Friedrich Tiedemann und Leopold Gmelin.[1]
Johannes Müller vermutete in Pepsin ein Enzym, das die Fleischverdauung fördert, und übernahm den von Eilhard Mitscherlich eingeführten Begriff „Kontakt-Ferment“.[1] Entdeckt wurde das Magenpepsin[2] als erstes tierisches Enzym im Jahr 1836 vom deutschen Physiologen Theodor Schwann.[3] 1839 wurde von Adolph Wasmann (1807–1853) eine Anleitung veröffentlicht, wie man Pepsin durch Fällung gewinnen kann. Friedrich Heinrich Bidder konnte schließlich beweisen, dass Salzsäure für den Magen vonnöten ist, dass er verdauen kann und dass das Pepsin durch die Salzsäure aktiviert werden muss.[1]
Boudault kannte die Versuche von Bidder nicht und muss so auch als Entdecker des Pepsinogens angesehen werden, da er zu denselben Ergebnissen kam.[1]
1874 wurde das Pepsinogen dann von Wilhelm Ebstein und Paul Grützner in der Magenschleimhaut nachgewiesen.[1]
Der Leibarzt von Napoleon III., Lucien Corvisart (1824–1882), nutzte den Magensaft von Tieren seit 1852, um Patienten mit Dyspepsie zu behandeln. Ihm wurde geraten, das Pepsin direkt nach der Methode von Wasmann herzustellen, um die Akzeptanz zu vergrößern. Auch in den Werken „Pharmacopoea germanica“ (1872) sind Monografien zu „Pepsinum“ und „Vinum Pepsini“ zu finden, die die Behandlung von gastrischen Verdauungsinsuffizienzen belegt. 1873 kam das erste Pepsin-Präparat von Friedrich Witte (Rostock) auf den Markt.[1]
1890 wurde ein Verfahren zur Pepsingewinnung in größerem Maßstab, z.B. aus 200 Schweinemägen, patentiert.[4] Das reine kristalline Pepsin wurde erstmals 1929 von John Howard Northrop, einem US-amerikanischen Chemiker, beschrieben.[5] 1898 benannte Caleb Bradham aus New Bern (North Carolina) das Erfrischungsgetränk „Pepsi Cola“ nach den wichtigsten Inhaltsstoffen Pepsin und Kolanussextrakt.
Eigenschaften
Pepsin ist eine saure Endopeptidase mit einer Molekülmasse von 36.000 Dalton. Es ist ein Phosphoprotein mit einer Länge von 327 Aminosäuren. Gebildet wird es unter Einwirkung der Salzsäure des Magens aus einer inaktiven Vorstufe, dem Pepsinogen. Die Spaltung findet ohne Einwirkung eines anderen Enzyms statt (Autoproteolyse).
Zwei Aspartate (Asparaginsäure) befinden sich als funktionelle Aminosäuren im aktiven Zentrum. Durch diese wird die Spaltung von Eiweißen in hochmolekulare, wasserlösliche Peptone katalysiert. Pepsin spaltet bevorzugt am N-Terminus von Phenylalanin, das häufigste Muster ist P/-/-/FL + -/R/L/-, das Katalyseverhalten ist also sequenzspezifisch.
Die höchste Aktivität hat Pepsin bei einem pH-Wert zwischen 1,5 und 3.
Oberhalb von pH 4 nimmt die Funktion des Enzyms signifikant ab. Ab einem pH von 7 wird das Enzym irreversibel denaturiert.[6]
Temperaturen bis 60 °C können seine Funktion nicht beeinträchtigen, ebenso wenig höhere Konzentrationen von Harnstoff und Guanidin. In gefriergetrocknetem Zustand kann Pepsin bei 4 °C einige Monate gelagert werden.
Verwendung
Pepsin eignet sich gut zur Untersuchung der Disulfidverbrückung in anderen Proteinen. Da die Spaltung bei niedrigen pH-Werten durchgeführt wird, ist die Gefahr von Disulfidaustauschreaktionen gering. Die kommerziell verfügbare Pepsin-Form ist meistens Pepsin aus dem Magen des Schweins.
Siehe auch
Einzelnachweise
- ↑ Hochspringen nach: a b c d e f Wolf-Dieter Müller-Jahncke, Christoph Friedrich, Ulrich Meyer: Arzneimittelgeschichte. 2., überarbeitete und erweiterte Auflage. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2005, ISBN 978-3-8047-2113-5, S. 112 f.
- ↑ Paul Diepgen, Heinz Goerke: Aschoff/Diepgen/Goerke: Kurze Übersichtstabelle zur Geschichte der Medizin. 7., neubearbeitete Auflage. Springer, Berlin/Göttingen/Heidelberg 1960, S. 36.
- ↑ Marcel Florkin: La découverte de la pepsine
par Théodore Schwann [Discovery of pepsin by Theodor Schwann]. In: Revue Médicale De Liège.
Band 12,
Nr. 5, 1. März 1957,
S. 139–144,
 PMID 13432398 (französisch).
PMID 13432398 (französisch).
- ↑ Patent
 US433395:
Obtaining Pepsin. Angemeldet am 3. April 1889, veröffentlicht am 29. Juli 1890,
Erfinder: John Brill.
US433395:
Obtaining Pepsin. Angemeldet am 3. April 1889, veröffentlicht am 29. Juli 1890,
Erfinder: John Brill.
- ↑ John H. Northrop: Crystalline Pepsin. In:
Science. Band 69,
Nr. 1796, 31. Mai 1929,
S. 580–580,
 PMID 17758437
(
PMID 17758437
( sciencemag.org)
sciencemag.org)
- ↑ John Del Valle : Peptic Ulcer and Related Disorders in Dan L. Longo, Anthony S. Fauci, Dennis L. Kasper, Stephen L. Hauser, J. Larry Jameson, Joseph Localzo (Hrsg.): Harrison's Principles of Internal Medicine. 18. Auflage, Band 2, New York, 2012, S. 2441


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 23.12. 2025