
Acetylchlorid
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
Acetylchlorid oder Essigsäurechlorid ist eine Chemikalie, genauer das funktionelle Chlorderivat der Essigsäure, in dem die Hydroxygruppe der Säure durch Chlor substituiert ist.
| Strukturformel | ||
|---|---|---|
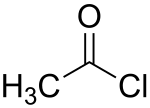
| ||
| Allgemeines | ||
| Name | Acetylchlorid | |
| Andere Namen |
| |
| Summenformel | C2H3ClO | |
| Kurzbeschreibung | farblose Flüssigkeit mit stechendem Geruch | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | ||
| EG-Nummer | 200-865-6 | |
| ECHA-InfoCard | ||
| PubChem | ||
| ChemSpider | ||
| DrugBank | ||
| Eigenschaften | ||
| Molare Masse | 78,50 g/mol | |
| Aggregatzustand | flüssig | |
| Dichte | 1,10 g/cm3 (20 °C) | |
| Schmelzpunkt | −112 °C | |
| Siedepunkt | 51 °C | |
| Dampfdruck | 309 hPa (20 °C) | |
| Löslichkeit | reagiert heftig mit Wasser | |
| Dipolmoment | 2,72(14) D (9,1 · 10−30 C · m) | |
| Brechungsindex | 1,3886 (20 °C) | |
| Thermodynamische Eigenschaften | ||
| ΔHf0 |
| |
Gewinnung und Darstellung
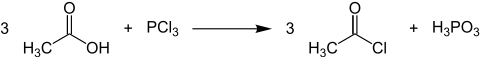
Acetylchlorid wird durch die Umsetzung von Calciumchlorid mit Essigsäureanhydrid hergestellt. Alternativ lässt es sich durch Umsetzung von Essigsäure mit Phosphor(III)-chlorid erhalten. Die Synthese aus Essigsäure und Thionylchlorid bzw. Phosphor(V)-chlorid ist ebenfalls möglich, liefert aber schlechtere Ausbeuten.
Eigenschaften
Acetylchlorid ist sehr flüchtig, es raucht an feuchter Luft infolge Bildung von HCl und besitzt eine heftige Reiz- bzw. Ätzwirkung auf die Atemwege. Wie alle Carbonsäurechloride ist Acetylchlorid sehr reaktionsfähig. Mit Wasser reagiert es rasch und exotherm unter Bildung von Essigsäure, mit Alkoholen und Phenolen unter Bildung der entsprechenden Ester und mit Ammoniak sowie primären und sekundären Aminen werden Amide gebildet. Dabei wird jeweils Chlorwasserstoff abgespalten.
Verwendung
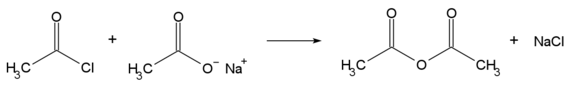
Acetylchlorid wird hauptsächlich zur Veresterung und Acetylierung in chemischen Synthesen benutzt. Aber auch bei der Synthese von Arzneimitteln (Acetylsalicylsäure) wird Acetylchlorid bei der Veresterung eingesetzt. Zusammen mit Natriumacetat kann es zur Darstellung von Essigsäureanhydrid benutzt werden:


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 28.10. 2023

