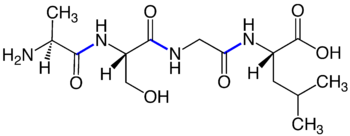
Peptidbindung
Eine Peptidbindung ist eine amidartige Bindung zwischen der Carboxygruppe einer Aminosäure und der Aminogruppe des α-Kohlenstoffatoms (α-C-Atom) einer zweiten Aminosäure. Zwei Aminosäuren können (formal) unter Wasserabspaltung zu einem Dipeptid kondensieren. Bei der Translation wird diese Reaktion von den Ribosomen katalysiert.
Formal reagieren beispielsweise zwei Moleküle der proteinogenen Aminosäure Alanin unter Wasserabspaltung zu dem Dipeptid Alanyl-Alanin:
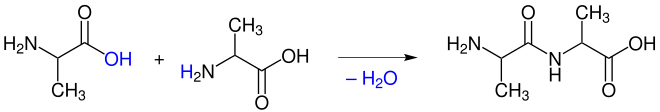
Da die Aminogruppe zu schwach nukleophil ist, um direkt mit der Carboxygruppe zu reagieren, bzw. auch protoniert als –NH3(+) vorliegen kann, liegt das Gleichgewicht unter Normbedingungen auf der linken Seite. Die chemische Reaktion ist endergon.
Sowohl bei der Laborsynthese von Peptiden als auch bei der biologischen Synthese von Peptiden und Proteinen müssen die reaktiven Gruppen zuerst aktiviert werden. Dies geschieht in biologischen Systemen zumeist durch Enzyme.
Durch mehrfache Kondensation bilden sich Tripeptide, Tetrapeptide, Polypeptide und schließlich Proteine, kettenförmige, aus Aminosäuren aufgebaute Makromoleküle. Polypeptidketten (bzw. Proteinketten) bilden das primäre Strukturelement der Proteine.
Zu Primär-, Sekundär- und Tertiärstrukturen von Peptiden und Proteinen siehe Proteinstruktur.
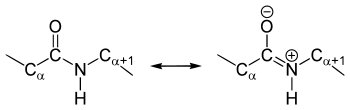
Die Kristallstrukturanalysen von Aminosäuren und Dipeptiden zeigen, dass die Amid-Gruppe planar ist, d. h. alle am Aufbau beteiligten Atome liegen in einer Ebene. Der Diederwinkel (HNCO) liegt bei 180° und die Atome können wegen Mesomeriestabilisierung nicht gegeneinander verdreht werden. In den nativen Proteinen liegen vorwiegend trans-Peptidbindungen vor, cis-Peptidbindungen finden sich vor allem in cyclischen Dipeptiden (Diketopiperazinen) und cyclischen Tripeptiden (Beispiel: Cyclotriprolyl). Der Grund für das häufige Auftreten von trans-Peptidbindungen liegt an den sterischen Hinderungen zwischen den Gruppen am α-C-Atom bei cis-Peptidbindungen, die bei der trans-Konformation nicht auftreten.
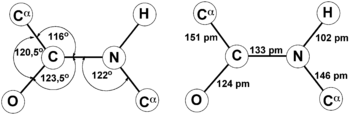
Die Bindungslängen sind zwischen Stickstoff und Carbonyl-Kohlenstoff 133 pm, zwischen Stickstoff und α-C-Atom 146 pm, zwischen Carbonyl-Kohlenstoff und α-C-Atom 151 pm und zwischen Carbonyl-Kohlenstoff und Sauerstoff 124 pm. Die geringere Länge der C-N-Bindung in der Amidbindung im Vergleich zur normalen C-N-Bindung weist darauf hin, dass sie Doppelbindungscharakter besitzt; diese Art der chemischen Bindung wird auch partielle Doppelbindung genannt. Diese Besonderheit findet ihre Erklärung in der Amid-Iminol-Tautomerie der Peptidbindung.
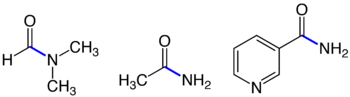
Peptide und Amide
Durch die Reaktion der Carboxygruppe einer Aminosäure und der Aminogruppe einer zweiten Aminosäure bildet sich unter Wasserabspaltung eine Peptidbindung. Jede Peptidbindung ist auch eine Amidbindung.
Voraussetzung für die Bildung einer Peptidbindung ist die Kondensationsreaktion der endständigen Carboxygruppe am C1-Atom mit der Aminogruppe am α-C-Atom einer zweiten Aminosäure. Jede andere Kondensation zwischen Carboxygruppe und Aminogruppe führt auch zu einer Amidbindung, die aber keine Peptidbindung ist.
Werden Peptide mittels Peptidbindungen verlängert, so reagieren die endständigen Carboxy- oder Aminogruppen am α-C-Atom mit weiteren Aminosäuren.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 08.05. 2024