
Volumenkontraktion
Der Begriff Volumenkontraktion wird insbesondere in der Chemie für eine Verkleinerung des Volumens beim Mischen von zwei Stoffen gebraucht.
Eine Volumenkontraktion (Volumenverminderung) tritt auf, wenn beim Mischen mehrerer Flüssigkeiten zu einer
Lösung
das Gesamtvolumen kleiner ist als die Summe der Volumina der einzelnen
Komponenten. Die Volumendifferenz wird Exzessvolumen
genannt und ist bei der Volumenkontraktion negativ. Sie ist bei vielen Lösungen
sehr gering oder praktisch nicht vorhanden.
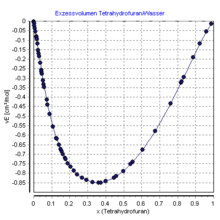
Merklich ist dieser Effekt jedoch bei einem Gemisch von Alkohol und Wasser. Mischt man beispielsweise 48 ml Wasser mit 52 ml Ethanol, so resultiert ein Gesamtvolumen von 96,3 statt von 100 ml. Die Verringerung des Volumens hängt nichtlinear vom Mischungsverhältnis ab (vgl. Abbildung), weshalb der Alkoholgehalt der Mischung nicht über Messungen des Volumens, sondern nur über solche von Dichte oder Siedepunkt bestimmt werden kann.
Ursache der Volumenkontraktion ist die Ausbildung zusätzlicher Bindungskräfte (Entstehen von Wasserstoffbrücken zwischen den Molekülen), wodurch diese einen kleineren Raum einnehmen. In der Ozeanografie gibt es einen ähnlichen, allerdings kleineren Effekt wegen des Salzgehalts im Meerwasser.
Einfluss auf Gehaltsangaben
Gibt man den Gehalt
einer Komponente in einer Lösung als Volumenkonzentration
an, so wird die Volumenkontraktion berücksichtigt.
Soll die Volumenkontraktion dagegen außer Betracht bleiben, wird der Gehalt
vorzugsweise als Volumenanteil
angegeben.
Volumendilatation
Es gibt auch Flüssigkeiten, die bei Mischung zu einer Volumendilatation, also einer Volumenvergrößerung, führen. In diesem Fall ist das Exzessvolumen positiv. Beispiele hierfür sind Mischungen aus Methylcyclohexan und 2-Pentanol oder aus Dichlormethan und 2-Butanon.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 30.05. 2024