Isentrop
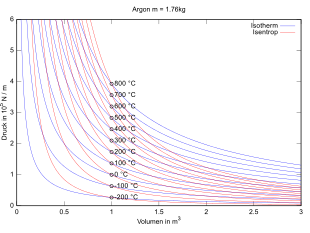
isentrope und isotherme Zustandsänderung
im p-V-Diagramm
im p-V-Diagramm
In der Thermodynamik
wird ein Prozess
bzw. eine Strömung
als isentrop bezeichnet, wenn sich die Entropie
 nicht ändert:
nicht ändert:
Als Isentrope bezeichnet man Linien gleicher Entropie. Da Entropie und potentielle Temperatur direkt miteinander in Beziehung stehen, wird der Begriff der Isentrope auch synonym für Linien gleicher potentieller Temperatur gebraucht.
Ein adiabatisch reversibler Prozess ist immer auch isentrop, die Umkehrung gilt aber nicht.
Die isentrope Zustandsänderung idealer Gase lässt sich durch die Poissonschen Gleichungen beschreiben:
dabei sind:
- v = spezifisches Volumen
- p = Druck
- T = absolute Temperatur
 = Isentropenexponent.
= Isentropenexponent.
Der Index 0 kennzeichnet den Ausgangszustand, die Größen ohne Index sind die Variablen.


© biancahoegel.de;
Datum der letzten Änderung: Jena, den: 08.08. 2020



