
Natriumhydrogensulfit
| Sicherheitshinweise | ||||||||
|---|---|---|---|---|---|---|---|---|
| ||||||||
| MAK | Schweiz: 5 mg/m3 (gemessen als einatembarer Staub)[5] | |||||||
| Toxikologische Daten | 1540 mg/kg (LD50, Ratte, oral)[6] | |||||||
Natriumhydrogensulfit (NaHSO3), auch Natriumbisulfit, ist ein Natrium-Salz der Schwefligen Säure. Es ist außerhalb von wässrigen Lösungen nicht stabil.
| Strukturformel | ||
|---|---|---|
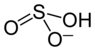
| ||
| Allgemeines | ||
| Name | Natriumhydrogensulfit | |
| Andere Namen | ||
| Summenformel | NaHSO3 | |
| Kurzbeschreibung | farblose bis gelbliche Flüssigkeit (existiert nur in Lösung)[3] | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | ||
| EG-Nummer | 231-548-0 | |
| ECHA-InfoCard | ||
| PubChem | ||
| ChemSpider | ||
| DrugBank | ||
| Eigenschaften | ||
| Molare Masse | 104,06 g/mol | |
Darstellung
Eine wässrige Lösung von Natriumdisulfit ergibt Natriumhydrogensulfit.
Schwefeldioxid durch eine Lösung von Natriumcarbonat leiten ergibt ebenfalls Natriumhydrogensulfit.
Eigenschaften
Im Handel befindet es sich als Lösung mit einem zwischen 37 und 50 % liegenden Gehalt an Natriumhydrogensulfit. Diese Lösungen weisen ätzende, reduzierende und stark bleichende Eigenschaften auf. Beim Konzentrieren der wässrigen Lösung entsteht Natriumdisulfit (Na2S2O5) bzw. Natriumsulfit.
Von Bedeutung ist die Additionsreaktion mit Aldehyden oder Ketonen zu sogenannten Hydrogensulfitaddukten (Bisulfitaddukten), wobei sich der Schwefel des Hydrogensulfitions nukleophil an die Carbonylgruppe unter Bildung eines Hydroxyalkylsulfonations anlagert. Als Beispiel ist hier die Reaktion mit Formaldehyd unter Bildung des schwerlöslichen Natriumhydroxymethylsulfonats demonstriert:
Die Hydrogensulfit-Addition wird häufig zur Aufreinigung von Aldehyden oder Ketonen verwendet, da sie unter basischen oder auch sauren Bedingungen reversibel ist.[7]
Verwendung
Als Lebensmittelzusatzstoff E 222 findet Natriumhydrogensulfit Verwendung als Konservierungsmittel z.B. bei der Stärke- und Zuckerherstellung, Antioxidationsmittel und als Stabilisator in Lebensmitteln sowie zur Analyse von Methylierungsmustern in DNA. Genutzt wird es auch als Reduktionsmittel in der chemischen Industrie zur Abwasserbehandlung. Es kommt auch in der Papierindustrie zum Einsatz. Es wird in der Sulfomethylierung zur Herstellung von waschaktiven Substanzen, Ionentauschern und wasserlöslichen Harzen verwendet. [8]
Einzelnachweise
- ↑ Eintrag zu
 E 222: Sodium hydrogen sulphite in
der Europäischen Datenbank für Lebensmittelzusatzstoffe.
E 222: Sodium hydrogen sulphite in
der Europäischen Datenbank für Lebensmittelzusatzstoffe.
- ↑ Eintrag zu
 SODIUM BISULFITE in der
CosIng-Datenbank
SODIUM BISULFITE in der
CosIng-Datenbank
- ↑ Hochspringen nach: a
b c Eintrag zu
 Natriumhydrogensulfit, wässrige Lösung in der
GESTIS-Stoffdatenbank des
IFA.(JavaScript erforderlich)
Natriumhydrogensulfit, wässrige Lösung in der
GESTIS-Stoffdatenbank des
IFA.(JavaScript erforderlich)
- ↑ Eintrag zu
 Sodium hydrogensulfite im
Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA).
Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung
Sodium hydrogensulfite im
Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA).
Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung
 erweitern.
erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva):
 Grenzwerte –
Aktuelle MAK- und BAT-Werte (Suche nach 7631-90-5 bzw. Natriumhydrogensulfit.
Grenzwerte –
Aktuelle MAK- und BAT-Werte (Suche nach 7631-90-5 bzw. Natriumhydrogensulfit.
- ↑ Datenblatt
 Natriumhydrogensulfit
bei Merck.
Natriumhydrogensulfit
bei Merck.
- ↑ Beyer-Walter: Lehrbuch der organischen Chemie, 23. Auflage, S. Hirzel Verlag, Stuttgart 1998.
- ↑ C. M. Suter, R. K. Bair, F. G. Bordwell: The sulfomethylation reaction. In: Journal of Organic Chemistry, 10.5, 1945, S. 470–478.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 18.11. 2025
