Vanadate
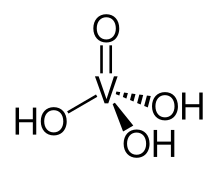
Vanadate sind die Salze der in freier Form nicht existenten Vanadium-Säuren HxVyOz. Die Vanadate selbst sind in wässriger Lösung stabil, wobei die auftretenden Formen vom pH-Wert der Lösung abhängen. Einige Vanadate kommen auch natürlich als Vanadiumminerale vor, so etwa Vanadinit, Descloizit und Carnotit.[1]
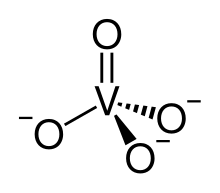
Darstellung
Viele Vanadate sind aus Vanadium(V)-oxid durch Erhitzen mit der entsprechenden Menge eines Metalloxids darstellbar:
- Calciumoxid und Vanadium(V)-oxid reagieren zu Calciumorthovanadat
- Dinatriumoxid und Vanadium(V)-oxid reagieren zu Tetranatriumdivanadat
Aus Vanadatlösungen können schwerlösliche Varianten – wie Ammoniummetavanadat – durch Umsetzung mit einem anderen Metallsalz ausgefällt werden:
- Ammoniumchlorid fällt aus einer wässrigen Natriummetavanadatlösung schwerlösliches Ammoniummetavanadat
Typen der Vanadate
Lösliche Vanadate
In wässrigen Lösungen können zahlreiche verschiedene Vanadationen vorhanden sein, wobei die Verteilung stark vom pH-Wert abhängig ist:[2]
- bei pH > 13 enthält die Lösung vorwiegend das tetraedrische Orthovanadat-Anion [VO4]3−
- zwischen pH 7 und 13 treten neben dem Orthovanadat auch das Divanadat oder Pyrovanadat [V2O7]4− und das Metavanadat [VO3]− auf; je niedriger der pH-Wert ist, desto höher ist der Anteil protonierter Anionen wie [HVO4]2− und [HV2O7]3−
- ab pH 7 sind vorwiegend orangefarbene Decavanadate [V10O28]6−, [HV10O28]5− und [H2V10O28]4− vorhanden.
Schwerlösliche Vanadate
Bei der technischen Vanadiumherstellung ist das Ammoniummetavanadat NH4VO3 von Bedeutung, das bei der Zugabe von Ammoniumsalzen aus Vanadatlösungen als schwerlösliche, gelbe, rhombische Plättchen bildende Verbindung ausfällt. Bei der Zugabe von Soda (Na2CO3) oder Sodalösung fällt ein ebenfalls gelbes, schuppiges Natriumorthovanadat Na3VO4 aus. Beide Salze, normalerweise in reinem Zustand weiße Verbindungen, sind jedoch durch einen geringen Gehalt an Polyvanadaten gelblich gefärbt.
Calciumvanadate sind durch Reaktion von Calciumoxid (CaO) mit Vanadium(V)-oxid (V2O5) darstellbar; das gewählte stöchiometrische Verhältnis bestimmt, ob dabei Ortho-, Pyro- oder Metavanadate entstehen.
Ähnlichkeit zu Phosphaten
Die verschiedenen Vanadate ähneln strukturell und in ihrer Chemie stark den Phosphaten; so sind ebenfalls alle Anionen aus (teils kondensierten) Tetraedern aufgebaut, wobei bei den kondensieren Vanadaten diese über eine Sauerstoffbrücke verbunden sind. Auch hier existieren für die Orthovanadate primäre (Dihydrogen-), sekundäre (Hydrogen-) und tertiäre (nicht protonierte) Formen. Die Divanadate und höheren Vanadate besitzen je nach der Anzahl Protonen, die aufgenommen werden können, auch quartäre und pentäre Formen.
| Primäre Vanadate (Di-/Trihydrogenvanadate) |
Sekundäre Vanadate (Di-/Hydrogenvanadate) |
Tertiäre Vanadate (Hydrogenvanadate) |
Quartäre Vanadate |
|---|---|---|---|
| Natriumdihydrogenorthovanadat, NaH2VO4 | Dinatriumhydrogenorthovanadat, Na2HVO4 | Natriumorthovanadat, Na3VO4 | n.v. |
| Natriumtrihydrogendivanadat, NaH3V2O7 | Dinatriumdihydrogendivanadat, Na2H2V2O7 | Trinatriumhydrogendivanadat, Na3HV2O7 | Tetranatriumdivanadat, Na4V2O7 |
Polyoxovanadate
Polyoxovanadate (POVs) gehören zur Gruppe der Polyoxometallate (POMs); sie bestehen im Allgemeinen aus mehreren [MOx]-Einheiten (mit M = V, Nb, Mo, Ta, W und x = 4 – 7). Meistens weisen sie eine oktaedrische oder quadratisch-pyramidale Koordinationsgeometrie auf. Die Metallzentren liegen häufig in einer d0- oder d1-Elektronen-Konfiguration vor. Die POVs weisen eine große Vielfalt an Spezies auf. Weiterhin besteht auch die Möglichkeit des Einbaus von Heteroatomen in Polyoxovanadatanionen. Oft sind in den Strukturen einige Vanadium-Atome durch beispielsweise Arsen, Antimon, Germanium oder Silicium ersetzt, so dass die sogenannten Heteropolyanionen gebildet werden. Weiterhin ist es möglich, organische Moleküle oder Übergangsmetall-Komplexe an die POVs zu binden. Daraus resultieren neue physikalische und chemische Eigenschaften.[3]
Im Gegensatz zu den Pendants mit Molybdän oder Wolfram werden Polyoxovanadate oftmals solvothermal hergestellt. Für die Entstehung der Polyoxovanadate sind sehr viele Syntheseparameter entscheidend, unter anderem auch der pH-Wert, da sich einzelne Spezies durch Änderung des pH-Wertes ineinander umwandeln können. Bei sehr hohem pH-Wert liegen so vorwiegend Orthovanadate [VO4]3− vor, die beim Ansäuern in Polyvanadate, wie z. B. Decavanadat [V10O28]6−, übergehen.[4]
Vanadatminerale
Die Gruppe der Vanadatminerale zeigt wegen Diadochie eine große Vielfalt ähnlicher Mineralien, bei denen jeweils Elemente ähnlicher Ionenradien und gleicher Ladungszahl ausgetauscht sein können.[1] Ein natürlich vorkommendes Vanadat ist das im hexagonalen Kristallsystem auftretende, rotgefärbte Vanadinit mit der chemischen Zusammensetzung Pb5(VO4)3Cl, das tonnenförmige Kristalle bildet.[5] Carnotit oder Uranglimmer ist ein vanadiumhaltiger, gelber bis grünlicher, monokliner Glimmer der Zusammensetzung K2(UO2)2(VO4)2·3H2O.[6] Descloizit kann unterschiedlich gefärbt sein,[7] und kristallisiert in orthorhombischen Kristallen mit der Zusammensetzung PbZn(VO4)(OH).
Biologische Bedeutung und Toxikologie
Obwohl Vanadium für den Stoffwechsel essentiell ist, hemmen Orthovanadate ([VO4]3−) in höheren Konzentrationen membrangebundene Enzyme (P-ATPasen, auch P-Typ-ATPasen) und sind deshalb für nahezu alle Eukaryoten und Prokaryoten giftig. Dies beruht auf der Ähnlichkeit des Vanadat- mit dem Phosphat-Anion. Einige Wasserlebewesen, wie etwa Seescheiden, sind in der Lage, Vanadate aus dem Meerwasser anzureichern. Diese Lebewesen enthalten größere Mengen von Metalloproteinen, den sogenannten Vanabinen, die Vanadium enthalten.[8]
Einzelnachweise
- ↑ Hochspringen nach: a b Vanadiumminerale. In: Lexikon der Geowissenschaften. Wissenschaft-Online-Lexika
- ↑ Vanadate. In: Lexikon der Chemie. Wissenschaft-Online-Lexika
- ↑ D.-L. Long, R. Tsunashima, L. Cronin: Angew. Chem. 2010, 122, 1780.
- ↑ Y. Hayashi: Coord. Chem. Rev. 2011.
- ↑
 Mineralienatlas: Vanadinit.
Mineralienatlas: Vanadinit.
- ↑
 Mineralienatlas: Carnotit.
Mineralienatlas: Carnotit.
- ↑
 Mineralienatlas: Descloizit.
Mineralienatlas: Descloizit.
- ↑ T Ueki, T Adachi, S Kawano, M Aoshima, N Yamaguchi, K Kanamori, H. Michibata:
Vanadium-binding proteins (vanabins) from a vanadium-rich ascidian Ascidia sydneiensis samea. In:
Biochim Biophys Acta. Band 1626,
Nr. 1–3, 2003,
S. 43–50,
doi:
 10.1016/S0167-4781(03)00036-8,
10.1016/S0167-4781(03)00036-8,
 PMID 12697328.
PMID 12697328.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 29.06. 2024