
Bariumoxid
| Sicherheitshinweise | ||||||||
|---|---|---|---|---|---|---|---|---|
| ||||||||
| MAK | 0,5 mg/m3 (Ba)[2] | |||||||
Bariumoxid ist das Oxid des Erdalkalimetalls Barium. Es besitzt die Formel BaO.
Bariumoxid (Baryterde) wurde zuerst von Johan Gottlieb Gahn in Zusammenarbeit mit Carl Wilhelm Scheele 1774 aus Schwerspat dargestellt[7]. Es wurde zunächst von Torbern Olof Bergman als Terra ponderosa (lateinisch für Schwererde) bezeichnet und erhielt später durch Richard Kirwan den Namen Baryt sowie die Bezeichnungen Baryta und Barya[8].
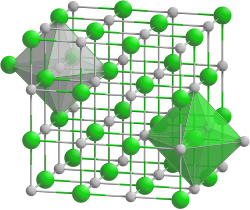
| Kristallstruktur | ||
|---|---|---|
| ||
| _ Ba2+ _ O2− | ||
| Kristallsystem | kubisch | |
| Raumgruppe | Fm3m (Nr. 225) | |
| Koordinationszahlen | Ba[6], O[6] | |
| Allgemeines | ||
| Name | Bariumoxid | |
| Verhältnisformel | BaO | |
| Kurzbeschreibung | farbloses Pulver[1] | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | | |
| EG-Nummer | 215-127-9 | |
| ECHA-InfoCard | | |
| PubChem | | |
| ChemSpider | | |
| Eigenschaften | ||
| Molare Masse | 153,32 g/mol | |
| Aggregatzustand | fest | |
| Dichte | 5,7 g/cm3[2] | |
| Schmelzpunkt | ca. 1920 °C[2] | |
| Siedepunkt | 2000 °C[3] | |
| Löslichkeit | In Wasser Zersetzung zu Bariumhydroxid[2] | |
| Brechungsindex | 1,9841[4] | |
| Thermodynamische Eigenschaften | ||
| ΔHf0 | −554 kJ/mol[6] | |
Eigenschaften
Bariumoxid ist ein farbloser Feststoff, der bei 1918 °C schmilzt. Mit Wasser reagiert es unter lebhafter Wärmeentwicklung zu Bariumhydroxid.
Er besitzt eine Kristallstruktur vom Natriumchlorid-Typ und reagiert mit feuchter Luft zum Hydroxid, mit CO2-haltiger Luft bildet sich Bariumcarbonat.[9]
Darstellung
Technisch wird es durch das Erhitzen eines Kohle-Bariumcarbonat-Gemisches auf etwa 1030 °C hergestellt, im Laboratorium auch durch Glühen von Bariumnitrat.[1]
Verwendung
Bariumoxid wird als Absorptionsmittel für Kohlenstoffdioxid und als Trocknungsmittel sowie zur Herstellung von Bariumperoxid, Bariumhydroxid, organischen Bariumsalzen, Spezialgläsern und Oxidkathoden verwendet.
Bariumoxid unterliegt an Sauerstoffatmosphäre einer Gleichgewichtsreaktion zu Bariumperoxid BaO2.
Zwischen 500 und 600 °C reagiert BaO zum Bariumperoxid. Oberhalb von 600 °C wird der im Peroxid gebundene Sauerstoff wieder abgegeben. BaO darf also nicht zu sehr erhitzt werden. Da die Gleichgewichtsreaktion zum Bariumperoxid mit Wärmeabgabe (exotherme Reaktion) und Volumenänderung verbunden ist, verschiebt sich das Gleichgewicht mit steigender Temperatur nach links. Man kann daher Sauerstoff bei niedriger Temperatur binden und bei höherer Temperatur wieder freisetzen.
Einzelnachweise
- ↑ Hochspringen nach: a b Eintrag zu
 Bariumoxid. In: Römpp Online. Georg Thieme Verlag,
abgerufen am 4. April 2026.
Bariumoxid. In: Römpp Online. Georg Thieme Verlag,
abgerufen am 4. April 2026.
- ↑ Hochspringen nach: a b c
d e f Eintrag zu
 Bariumoxid in der GESTIS-Stoffdatenbank des Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung, abgerufen am 4. April 2026. (JavaScript erforderlich)
Bariumoxid in der GESTIS-Stoffdatenbank des Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung, abgerufen am 4. April 2026. (JavaScript erforderlich)
- ↑ Datenblatt
 Bariumoxid
bei Thermo Fisher Scientific Inc., abgerufen am 4. April 2026.
Bariumoxid
bei Thermo Fisher Scientific Inc., abgerufen am 4. April 2026.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Index of Refraction of Inorganic Crystals, S. 10-245.
- ↑ Nicht explizit in Verordnung (EG)
Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag
 barium salts, with the exception of barium sulphate, salts of 1-azo-2-hydroxynaphthalenyl
aryl sulphonic acid, and of salts specified elsewhere in this Annex in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur
(ECHA), abgerufen am 4. April 2026. Hersteller bzw. Inverkehrbringer
können die harmonisierte Einstufung und Kennzeichnung
barium salts, with the exception of barium sulphate, salts of 1-azo-2-hydroxynaphthalenyl
aryl sulphonic acid, and of salts specified elsewhere in this Annex in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur
(ECHA), abgerufen am 4. April 2026. Hersteller bzw. Inverkehrbringer
können die harmonisierte Einstufung und Kennzeichnung  erweitern.
erweitern.
- ↑ PAETEC Formelsammlung Ausgabe 2003, S. 116.n
- ↑ Baryumoxyd. In: Joseph Kürschner (Hrsg.): Pierer’s Konversations-Lexikon. 7. Auflage. Band 2. Berlin, Stuttgart 1889, S. 500.
- ↑ Baryumoxyd. In: Joseph Kürschner (Hrsg.): Pierer’s Konversations-Lexikon. 7. Auflage. Band 2. Berlin, Stuttgart 1889, S. 500.
- ↑ Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 926.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 09.04. 2026

