
Nitrosamine
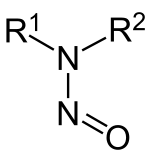
Nitrosamine, genauer N-Nitrosamine, sind eine Stoffklasse organisch-chemischer Verbindungen der allgemeinen Strukturformel R1R2N-NO, dabei sind R1 und R2 kohlenstoffhaltige Reste. Nitrosamine wirken karzinogen. Sie haben keine großtechnische Bedeutung.
Eigenschaften
Bei Raumtemperatur sind Nitrosamine üblicherweise flüssig oder fest. Durch die N−N=O-Gruppierung sind sie gut in Wasser und anderen polaren Lösungsmitteln löslich. Die Dichte variiert zwischen 0,9 und 1,2 g pro cm³.
Entstehung
Nitrosamine entstehen durch Anwesenheit nitrosierender Agentien (Salpetrige Säure, Stickstoffoxide), beispielsweise aus Aminen. Sie werden nur unter bestimmten Voraussetzungen gebildet, vor allem im sauren Milieu, wie es etwa im menschlichen Magen herrscht.
Nitrit bildet zunächst HNO2. Diese spaltet sich nach erneuter Protonierung in ein Nitrosyl-Kation (NO+) und Wasser auf [siehe (1)]. Das Nitrosyl-Kation reagiert mit einem Amin zum Nitrosamin weiter [siehe (2)].
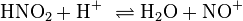 (1)
(1)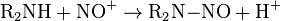 (2)
(2)
In der Atmosphäre bilden sich Nitrosamine auch photochemisch aus geeigneten Aminen durch Einwirkung von Stickstoffoxiden. Die unvollständige Verbrennung stickstoffreicher Materialien führt ebenfalls zur Bildung von Nitrosaminen. Sie bilden sich ebenfalls endogen (im menschlichen Körper), einerseits im sauren Milieu des Magens, andererseits auch durch körpereigene Bakterien.
Vorkommen
Hinweise für das Vorliegen von Nitrosaminen in Lebensmitteln pflanzlicher Herkunft, in Böden oder im Grundwasser gibt es nicht. Sie kommen – üblicherweise in sehr geringen Dosen – in vielen Lebensmitteln vor, beispielsweise in Bier, Fischen, gepökelten Fleischerzeugnissen oder in Käse. N-Nitrosamine sind Reaktionsprodukte von Nitrit und sekundären Aminen (wie in Proteinen), die vor allem unter Hitzeeinwirkung gebildet werden. Beim Erhitzen gepökelter Lebensmittel sowie beim Wiederaufwärmen von Spinat, dessen intrazelluläre Nitratdepots mikrobiell zu Nitrit umgewandelt wurden, besteht ebenfalls die Gefahr der Nitrosaminbildung.
Nitrosamine lassen sich auch in Latex-Matratzen, Luftballons und Tabak nachweisen.
Nitrosamine können auch in wassergemischten Kühlschmiermitteln
– aus in Nitrit umgewandeltem Nitrat
aus dem Ansetzwasser und eingeschleppten Aminen (Lebensmittelreste, Zigaretten)
– entstehen. Leitkomponente ist N-Nitroso-diethanolamin (NDELA), 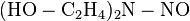 .
.
Auswirkungen auf die Gesundheit
Im Tierversuch wurde in sämtlichen Spezies eine stark krebserzeugende Wirkung bei 90 % der untersuchten Nitrosamine nachgewiesen. Nitrosamine sind Präkanzerogene, das heißt, sie müssen im Körper aktiviert werden, damit sie ihre schädliche Wirkung entfalten können. Dies erfolgt durch eine Cytochrom-P450-katalysierte Reaktion. In nachfolgenden Reaktionen werden das sehr reaktive Formaldehyd sowie Carbeniumionen freigesetzt, die eine stark gentoxische Wirkung haben.
Epidemiologische Studien deuten auf eine positive Korrelation zwischen Nitrit- und Nitrosaminaufnahme und Magenkarzinom, sowie zwischen dem Verzehr von Fleisch- und Wurstwaren und Magen- und Speiseröhrenkrebs hin.
Weitere epidemiologische Studien sehen zudem eine Korrelation zwischen dem zunehmenden Einsatz von Nitrat und Nitrit in Landwirtschaft (Düngung) und Nahrungsmittelindustrie (Konservierungsmittel), der dadurch erhöhten Belastung mit Nitrosaminen und der steigenden Zahl von Alzheimer-, Parkinson- und Diabetesfällen
Nitrosamine haben im Tierversuch auch Schäden der Leber und des Erbgutes hervorgerufen.
Nitrosodialkylamine (R1, R2 = Alkylrest) werden im Körper zu Alkyldiazohydroxiden metabolisiert, welche die ultimalen Kanzerogene darstellen, also die eigentlich krebserzeugende Wirkung haben. Diese zerfallen unter Stickstoffabgabe zu hochreaktiven Carbeniumionen, welche Addukte mit DNA, RNA und Proteinen bilden können. N-Nitrosodimethylamin beispielsweise methyliert die DNA-Basen Guanin und Adenin.
Nachweis
Nachgewiesen werden Nitrosamine unter anderem durch einen Chemilumineszenz-Detektor oder nach einer hochauflösenden Massenspektroskopie, jeweils nach Trennung durch Gaschromatografie.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 29.01. 2024