
Zintl-Phasen
Zintl-Phasen sind intermetallische Verbindungen zwischen wenig elektronegativen Alkalimetallen oder Erdalkalimetallen und mäßig elektronegativen Elementen aus der 11. bis 16. Gruppe des Periodensystems. Ihr Name wurde nach Eduard Zintls Tod von Fritz Laves zu Ehren Zintls vorgeschlagen und schnell akzeptiert.
In diesen Verbindungen wird das Elektron formal dem elektronegativeren Element zugeschrieben. Das aufgebaute Anionen-Teilgitter entspricht nach E. Busmann und Wilhelm Klemm dem einer Elementstruktur der gleichen Valenzelektronenkonfiguration. Die Zintl-Grenze bzw. -Linie kann dabei zwischen der 13. und der 14. Gruppe gezogen werden, sie trennt die salzartigen Phasen von den legierungsartigen Phasen der 11. bis 13. Gruppe.
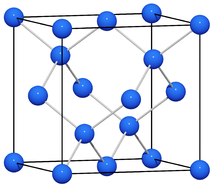
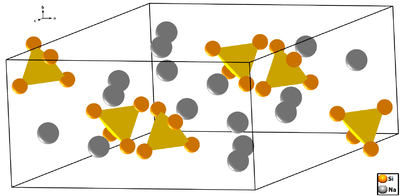
So entspricht zum Beispiel die Struktur des Thallium-Anionenteilgitters in Natriumthallid (NaTl) dem kubisch-flächenzentrierten Gitter, wobei die Hälfte der Tetraederlücken nochmals von Tl-Atomen besetzt ist. Die Natrium-Kationen sitzen in der anderen Hälfte der Tetraederlücken sowie in den Oktaederlücken des Kristallgitters. Ein weiteres Beispiel ist Natriumsilicid (NaSi), das in Analogie zu weißem Phosphor Si44−-Tetraeder bildet.
Viele Zintl-Phasen sind aufgrund der teilweise kovalenten, teilweise ionischen Bindungen mit daraus resultierender relativ kleiner Bandlücke (< 1 eV) diamagnetische Halbleiter, deren Leitfähigkeit im Gegensatz zu metallischen Leitern mit steigender Temperatur ansteigt.
Polyanionen
Zintl-Phasen werden nach der von Zintl aufgestellten und durch Klemm erweiterten Regel als ionische Verbindungen formuliert. Dabei sind Zintl-Phasen stark heteropolar, weisen aber oft die Eigenschaften eines schlechten Metalls auf (elektrische Leitfähigkeit, metallischer Glanz etc.). Für die Diskussion der Strukturen ist die formale ionische Auffassung jedoch sehr gut geeignet. Mit dem formalen Elektronenübertrag vom elektropositiven Metall M zum elektronegativen Partner E, erhält man Anionen, deren Struktur der 8-N Regel folgen. Damit ergeben sich Element-Element Bindungen und es wird eine polyanionische Struktur ausgebildet.
Beispiele
- NaSi: Si−: pseudo-Phosphor: [Si4]4−-Tetraeder
- CaSi: Si2−: pseudo-Schwefel: Si-Ketten (vgl. μ-Schwefel)
- Ca2Si: Si4−:pseudo-Argon: isolierte Si-Atome in der Struktur
- Ba3Si4: [Si4]6−: 2x Si− 2x Si2−: verzerrte Tetraeder mit zwei 2-bindigen und zwei 3-bindigen Silizium-Atomen
Hydride
Es gibt eine Reihe von Zintl-Phasen, die auch Wasserstoff in ihrer Struktur enthalten. Dabei unterscheidet man Zintl-Phasen Hydride, bei denen der Wasserstoff als H− vorliegt und die ausschließlich vom elektropositiven Metall koordiniert sind, und Polyanionische Hydride, die im Polyanion neben Element-Element Bindungen auch Element-Wasserstoff Bindungen aufweisen. In polyanionischen Hydriden ist der Wasserstoff i.d.R. der elektronegativere Partner, wodurch ihm die Oxidationsstufe -I zukommt.
Literatur
- Herbert Schäfer, Brigitte Eisenmann, Wiking Müller: Zintl‐Phasen: Übergangsformen zwischen Metall‐und Ionenbindung. In: Angew. Chem. 85, Nr. 17, 1973, S. 742–760, doi:10.1002/ange.19730851704.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 31.03. 2023