310-Helix
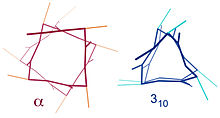
Die 310-Helix (3 Aminosäuren pro 360°-Drehung, 10-gliedriger Ring durch Wasserstoffbrückenbindung) ist ein Sekundärstruktur-Motiv von Peptiden und Proteinen. Diese Helix kann an den Enden von α-Helices wie auch separat vorkommen und etwa 10 % des Helix-Anteils von globulären Proteinen ausmachen. Sie ist eine rechtshändige Helix mit drei Aminosäureseitenketten pro Umdrehung. Die 310-Helix wird durch intramolekulare C=O•••H-N Wasserstoffbrückenbindungen zwischen der n-ten und der (n+3)-ten Aminosäure stabilisiert. Durch diese Wasserstoffbrückenbindung wird ein Ring mit zehn Bindungen gebildet, der der Struktur einer β-Schleife des Subtyps III entspricht. Häufig kommen nur kurze 310-Helices mit zwei bis drei Wasserstoffbrückenbindungen vor, denn die Ausbildung von Van-der-Waals-Kontakten und Wasserstoffbrückenbindungen ist weniger günstig als bei einer α-Helix.
Literatur
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6 Auflage, Spektrum Akademischer Verlag, Heidelberg 2007. ISBN 978-3-8274-1800-5.
- Donald Voet, Judith G. Voet: Biochemistry. 3. Auflage, John Wiley & Sons, New York 2004. ISBN 0-471-19350-X.
- Bruce Alberts, Alexander Johnson, Peter Walter, Julian Lewis, Martin Raff, Keith Roberts: Molecular Biology of the Cell, 5. Auflage, Taylor & Francis 2007, ISBN 978-0-8153-4106-2.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 19.07. 2023