
Agonist (Pharmakologie)
Als Agonist (von altgriechisch αγωνιστής agonistēs „der Tätige, Handelnde, Führende“) wird in der Pharmakologie eine Substanz (Ligand) bezeichnet, die durch Besetzung eines Rezeptors die Signaltransduktion in der zugehörigen Zelle aktiviert. Ein Agonist kann sowohl eine körpereigene Substanz sein (z. B. ein Hormon oder ein Neurotransmitter) als auch ein nicht-körpereigener Wirkstoff, der einen bestimmten Botenstoff in seiner Wirkung imitiert bzw. ersetzt. Chemische Verbindungen, die zwar an einen Rezeptor binden, diesen aber nicht aktivieren und somit blockieren und hemmend wirken, bezeichnet man dagegen als Antagonist.
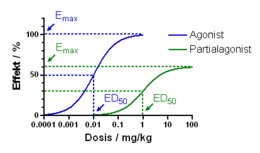
Anhand des Ausmaßes der Aktivierung kann zwischen einem vollen Agonisten und einem Partialagonisten unterschieden werden. Inverse Agonisten, die zu einer Inaktivierung eines spontanaktiven Rezeptors führen und somit einen zu vollen und partiellen Agonisten gegensätzlichen Effekt zeigen, werden hingegen nicht den Agonisten zugeordnet.
Das Ausmaß der Aktivierung eines Rezeptors hängt dabei nicht nur von den Eigenschaften des Liganden ab, sondern ist auch vom Ausmaß der Expression des Rezeptors in den untersuchten Zellen bzw. im untersuchten Gewebe abhängig.[1] Darüber hinaus sind einige Agonisten über denselben Rezeptor in der Lage, verschiedene Signalwege unterschiedlich stark zu aktivieren und somit – je nach untersuchtem Signal – unterschiedlich ausgeprägte Effekte zu erzeugen. Sie können also – je nach untersuchtem Signal – gleichzeitig volle Agonisten, Partialagonisten, stille Antagonisten oder inverse Agonisten sein. Derartige Agonisten werden auch als proteusartig oder funktionell-selektiv bezeichnet.[2][3]
Beispiele
Die folgende Tabelle zeigt Beispiele für Rezeptoren bzw. deren Subtypen und ihre Agonisten an der orthosterischen Bindungsstelle.
| Rezeptor | Subtyp | Agonist[legende 1] endogen; exogen |
|---|---|---|
| Acetylcholinrezeptoren | M1-5 | Acetylcholin; Carbachol, Muscarin |
| N1-2 | Acetylcholin; Nikotin | |
| Adrenozeptoren | α1A,B,D | Adrenalin, Noradrenalin; Phenylephrin |
| α2A-C | Adrenalin, Noradrenalin; Clonidin | |
| β1-3 | Adrenalin; Isoprenalin | |
| Dopaminrezeptoren | D1-5 | Dopamin |
| Histaminrezeptoren | H1-4 | Histamin |
| Opioidrezeptoren | μ1,2 | β-Endorphin; Casein, MorphinV, BuprenorphinP, Dermorphin[4] |
| κ1-3 | Dynorphine; Enadolin | |
| δ1,2 | β-Endorphin, Enkephaline, Deltorphine | |
| Serotoninrezeptoren | 5-HT1A-F, 5-HT5A, 5-HT7 | Serotonin; 5-Carboxamidotryptamin |
| 5-HT2A-C | Serotonin; α-Methylserotonin | |
| 5-HT3 | Serotonin; 2-Methylserotonin | |
| 5-HT4 | Serotonin; 5-Methoxytryptamin | |
| 5-HT6 | Serotonin; EMDT[5] | |
| 5-HT7 | Serotonin; N-Methylserotonin |
- Tabellenlegende
- ↑ endogen = Mediator im menschlichen Körper, exogen = körperfremder Überträgerstoff; V = Vollagonist, P = Partialagonist, Ak = besonders hohe agonistische Aktivität; FS = dezidierte funktionelle Selektivität ist bekannt; Sp = Subtypspezifisch (so weit bekannt); rN, sN = Namensgebend für den Rezeptor bzw. Subtyp (bei exogenen Agonisten oder nichttrivialen Fällen); Af = extrem affin; Rvi = Radioagonist, Nutzung in vivo; Rvt = überwiegende Nutzung in vitro (siehe auch PET, Tracer, Bindungsstudie)
Wiederaufnahmehemmer
Ähnlich wie Agonisten können auch Wiederaufnahmehemmer wirken. Sie sorgen dafür, dass Substanzen länger im synaptischen Spalt bleiben und so eine agonistische Wirkung haben. Ein Beispiel dafür sind die Antidepressiva.
Literatur
- Klaus Aktories, Ulrich Förstermann u. a.: Allgemeine und spezielle Pharmakologie und Toxikologie. 10. Auflage. Urban & Fischer, 2009, ISBN 978-3-437-42522-6, S. 8–13. eingeschränkte Vorschau in der Google-Buchsuche
Einzelnachweise
- ↑ D. Hoyer, H. W. Boddeke: Partial agonists, full agonists, antagonists: dilemmas of definition. In:
Trends Pharmacol. Sci. 14, 1993, S. 270–275.
 PMID 8105597.
PMID 8105597.
- ↑ T. Kenakin: Inverse, protean, and ligand-selective agonism: matters of receptor conformation. In:
FASEB J. 15, 2001, S. 598–611.
 PMID 11259378.
PMID 11259378.
- ↑ J. D. Urban, W. P. Clarke, M. von Zastrow, D. E. Nichols, B. Kobilka, H. Weinstein, J. A. Javitch, B. L. Roth,
A. Christopoulos, P. M. Sexton, K. J. Miller, M. Spedding & R. B. Mailman: Functional selectivity and classical concepts of quantitative pharmacology. In: J. Pharmacol. Exp.
Ther. 320, 2007, S. 1–13.
 PMID 16803859.
PMID 16803859.
- ↑
 Dermorphin.
Thermo Fisher (Kandel) GmbH (SICHERHEITSDATENBLATT)
Dermorphin.
Thermo Fisher (Kandel) GmbH (SICHERHEITSDATENBLATT)
- ↑ P. Svenningsson u. a.: Biochemical and behavioral evidence for antidepressant-like effects of 5-HT6 receptor
stimulation. In: J Neurosci. 27(15), 2007, S. 4201–4209.
 PMID 17428998.
PMID 17428998.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 13.02. 2026