
Chromsäure
| Sicherheitshinweise | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||
| Zulassungsverfahren unter REACH | besonders besorgniserregend: krebserzeugend (CMR); zulassungspflichtig | ||||||||||
| MAK |
| ||||||||||
Chromsäure mit der Struktur H2CrO4 existiert nur in verdünnten wässrigen Lösungen. Reine, wasserfreie Chromsäure ist unbekannt. Sie ist eine starke zweiprotonige Säure und bildet als Salze die Chromate. Hydrogenchromate sind hingegen instabil und nur in wässriger Lösung bekannt.
Wird Chromsäure als Feststoff angeboten, handelt es sich stets um das Anhydrid der Chromsäure, das Chromtrioxid. Ebenso wie das Anhydrid ist die Chromsäure ätzend und giftig.
| Strukturformel | |
|---|---|
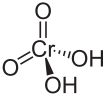 | |
| Allgemeines | |
| Name | Chromsäure |
| Andere Namen |
Dihydrogenchromat (IUPAC) |
| Summenformel | H2CrO4 |
| Kurzbeschreibung | dunkelrote bis gelbe geruchlose wässrige Lösung |
| Externe Identifikatoren/Datenbanken | |
| CAS-Nummer | 7738-94-5 |
| EG-Nummer | 231-801-5 |
| ECHA-InfoCard | 100.028.910 |
| PubChem | 24425 |
| Eigenschaften | |
| Molare Masse | 116,95 g/mol |
| Aggregatzustand | nur als Lösung in Wasser beständig |
| Dichte | 1,5 g/cm3 (50 % CrO3) |
| Siedepunkt | thermische Zersetzung |
| Löslichkeit | CrO3 gut löslich in Wasser: 1854 g/l (bei 20 °C) |
Wässrige Lösung
Chromsäure ist eine starke Säure (pKs-Wert: −0,61) und liegt im Gleichgewicht nur zu einem sehr geringen Teil als H2CrO4 vor. HCrO4− ist hingegen eine schwache Säure (pKs-Wert: 6,45). Daher liegt Chromsäure in verdünnter wässriger Lösung überwiegend als Hydrogenchromat HCrO4− vor.
Werden die wässrigen Lösungen mit einer Base versetzt, liegen bei einem pH-Wert > 7 überwiegend CrO42−-Ionen vor.
Bei pH-Werten zwischen 2 und 6 liegen HCrO4− vor und es
bilden sich in einer Gleichgewichtsreaktion Dichromate
(Cr2O72−). Bei dieser Reaktion kommt es zu
einem Farbumschlag von gelb nach orange. Ist der pH-Wert der Lösung < 1,
bilden sich unter weiterer Farbvertiefung Polychromate der allgemeinen Formel
CrnO3n+12−.
Verwendung
Chromsäure wird in der Chemie als Oxidationsmittel eingesetzt. Mit ihr lassen sich primäre Alkohole zu Aldehyden bzw. zu Carbonsäuren, sekundäre Alkohole zu Ketonen oxidieren.
In der Galvanotechnik wird Chromsäure zur Passivierung galvanisch erzeugter Schichten – vorwiegend bei Cadmium – und zur Vorbehandlung von Aluminiumoberflächen per anodischer Oxidation verwendet. Sie ist außerdem Hauptbestandteil der galvanischen Chromelektrolyte, die zum Verchromen verwendet werden. Des Weiteren werden Chromsäure bzw. Chromtrioxid zur Herstellung von Kaliumdichromat, Ammoniumdichromat und Chromdioxid verwendet.
Chromsäurelösungen werden ferner häufig für die rasche Feststellung verwendet, ob im Metall bzw. einer Legierung Silber vorliegt. Der Gegenstand der Probe wird hierbei vor der Prüfung aus Gründen anzunehmender Versilberung z. B. angefeilt und dieser Stelle mit der Säure aufgetupft. Die Säure ergibt mit Silber einen Silberchromat-Niederschlag in blutroten Farbtönen. Bei unedlen Metallen bildet sich kein Silberchromat. Je dunkler der blutrote Farbniederschlag ausfällt, desto höher ist der Silberfeingehalt.
Chromsäure ist nicht zu verwechseln mit der Chromschwefelsäure.
Toxikologie
Chromsäure ist äußerst giftig (die letale Dosis entspricht 1 bis 2 g) und auch seit langem als krebserregend bekannt. Bei Hautkontakt erzeugen sie Irritationen an Augen, Haut und Schleimhäuten. Chronischer Kontakt mit Chromsäure kann bei unterlassener Behandlung zu bleibenden Schäden führen.
Chromsäure kann zu einem toxischen Lungenödem und trotz späterer Behandlung zum Tod führen. Nach einer vorübergehenden Freiheit von Beschwerden (bis zu 48 Stunden) kann das Vollbild mit Hämoptoe, Zyanose, Aspiration oder Herzstillstand auftreten.
Seit 1958 empfiehlt die Weltgesundheitsorganisation (World Health Organization) für Chrom(VI)-Verbindungen eine maximal zulässige Konzentration von 0,05 mg/Liter im Trinkwasser.


© biancahoegel.de;
Datum der letzten Änderung: Jena, den: 02.04. 2023




