
Hessscher Wärmesatz
Der Hess’sche Wärmesatz (auch Satz von Hess) dient der Berechnung von Enthalpieänderungen bei chemischen Reaktionen. Er wurde 1840 von Germain Henri Hess aufgestellt.
In vielen Fällen können Produkte einer chemischen Reaktion auf verschiedenen Wegen entstehen. Der Reaktionsweg hat dabei nach dem Energieerhaltungssatz keinen Einfluss auf die Energie, die bei einer Reaktion aufgenommen oder abgegeben wird. Nach dem Hess’schen Wärmesatz gilt dasselbe für die Enthalpie einer chemischen Reaktion.
Aussage
Die Enthalpieänderung
eines Gesamtprozesses ist die Summe
der Enthalpieänderungen der einzelnen Prozessschritte. Unter Annahme von
Standardbedingungen ist die Standardreaktionsenthalpie eines Stoffes die
Differenz aus der Standardbildungsenthalpie der Produkte minus der
Standardbildungsenthalpie der Edukte:
Daraus folgt, dass die Reaktionsenthalpie nicht vom Reaktionsweg, sondern nur vom Anfangs- und vom Endzustand des Systems abhängt.
Erweiterungen
Man kann den Hess’schen Satz auf die Gibbs-Energie erweitern:
Des Weiteren ist auch die Entropieänderung mit dem Hess’schen Satz berechenbar. Man beachte, dass Entropie die Einheit Joule pro Kelvin besitzt und eine absolute Größe ist (kein Delta in der Summe!):
Beispiel
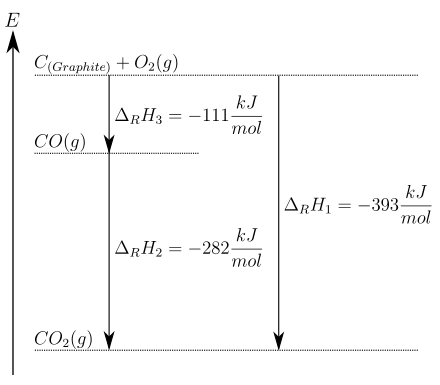
Graphit kann direkt zu Kohlenstoffdioxid verbrannt werden (1) oder indirekt über die Zwischenstufe Kohlenstoffmonoxid (2), (3):
Die Gesamtreaktionsenthalpie
ist in beiden Fällen gleich:
Literatur
- Chemie heute Sekundarbereich II, Schroedel Verlag, 1998, ISBN 3-507-10630-2.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 10.08. 2020