
Thrombozyt
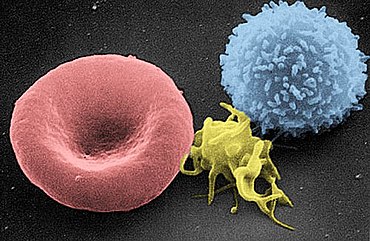
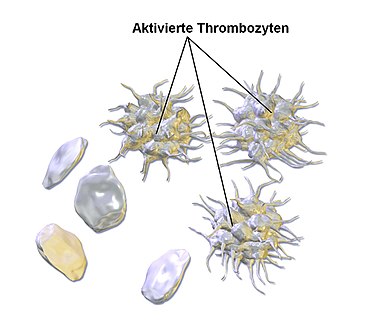
Der Thrombozyt oder Thrombocyt (von altgriechisch θρόμβος thrómbos „Klumpen“ sowie altgriechisch κύτος kýtos „Höhlung“, „Gefäß“, „Hülle“[1]) oder das Blutplättchen ist die kleinste Zelle des Blutes. Thrombozyten spielen eine wichtige Rolle bei der Blutgerinnung, indem sie sich bei der Verletzung eines Blutgefäßes an das umliegende Gewebe anheften („Thrombozytenadhäsion“) oder aneinanderheften („Thrombozytenaggregation“), sodass die Verletzung verschlossen wird. Zusätzlich setzen sie dabei gerinnungsfördernde Stoffe frei.
Blutplättchen haben weder Zellkerne noch Erbinformation (DNA). Sie entstehen durch Abschnürung aus Megakaryozyten, die sich im Knochenmark befinden.
Struktur und Funktion
Thrombozyten entstehen im Knochenmark, wo sie von Megakaryozyten, riesigen thrombozytenbildenden Zellen, abgeschnürt werden. Bis zu 8000 Thrombozyten können sich im Laufe eines Lebens von solch einer Knochenmarkszelle abschnüren. Dieser Vorgang wird Thrombopoese genannt und durch das Hormon Thrombopoietin unterstützt.
Thrombozyten haben einen Durchmesser von 1,5 µm bis 3,0 µm und sind scheibenartig flach (discoid). Während der Blutgerinnung ändern die Thrombozyten durch Aktivatoren wie ADP, Kollagen, Thromboxan und Thrombin ihre Form. Es erfolgt die Ausstülpung von Pseudopodien, was mit einer mehrfachen Oberflächenvergrößerung einhergeht. Dies begünstigt die Thrombusbildung durch fibrinvermittelte Bindung mit anderen Thrombozyten. Dieser Vorgang beschreibt die Funktion von Thrombozyten und wird Thrombozytenaggregation genannt.
Bei gesunden Personen gilt eine Thrombozytenanzahl zwischen 150.000 und 450.000 pro µl Blut als Normalwert. Die Thrombozyten-Konzentration ist individuell genetisch bedingt und variiert über die Lebenszeit eines gesunden Erwachsenen wenig. In einer gesunden Population folgt die Thrombozytenkonzentration einer Normalverteilung.[2]
Die durchschnittliche Lebensdauer von Thrombozyten beträgt acht bis zwölf Tage. Der Abbau erfolgt hauptsächlich in der Milz, in der auch ein Drittel der Thrombozyten temporär gespeichert ist, sowie in der Lunge und, in geringerem Maße, in der Leber.
Zelluläre Aspekte
Trotz Fehlens eines Zellkerns wurde in Thrombozyten mRNA aus Megakaryozyten gefunden. Sie sind daher, wenn auch begrenzt, zur Neusynthese von Proteinen befähigt. Sie besitzen wie andere Zellen Mitochondrien, jedoch eine spezielle Form des rauen Endoplasmatischen Retikulums (rER), das kanalikuläre System. Es dient als Calciumionen-Speicher, dessen rasche Entleerung ins Zytosol eine essentielle Voraussetzung für die physiologische Thrombozytenaggregation ist. Als weitere Kompartimente sind bei Thrombozyten die Speicher-Granula bedeutsam: Sie werden in α-Granula, elektronendichte Granula und Lysosomen unterteilt und enthalten aggregationsfördernde Substanzen und Proteine, deren Sekretion (Ausschüttung) für die Thrombozytenfunktion notwendig ist. Die Plasmamembran von Thrombozyten enthält unter anderem das Protein Gewebefaktor (engl. tissue factor). Man geht davon aus, dass sich Vesikel mit diesem Protein abschnüren und nun als zirkulierende Mikropartikel im Blut zu finden sind.[3] Durch diese Fähigkeit, die sie mit Monozyten gemein haben, unterstützen sie die Blutgerinnung.
Eine Milzvergrößerung (Splenomegalie) oder eine Immunthrombozytopenie führen zu einer Verringerung der durchschnittlichen Thrombozytenlebensdauer, was bei einer gleichbleibenden Produktionsrate zu einer insgesamt geringen Thrombozytenkonzentration führt. Umgekehrt kommt es nach Entfernung der Milz (Splenektomie) zu einem starken Anstieg der Thrombozytenanzahl durch das Fehlen des milzvermittelten Abbaus.
Pathologie der Blutplättchen
Bei den Blutplättchen gibt es drei Arten der Störung oder Abweichung. Unterschieden werden dabei primäre (meist genetisch bedingte) Abweichungen, die manchmal auch idiopathisch oder essentiell genannt werden, von sekundären Abweichungen aufgrund einer anderen zugrundeliegenden Erkrankung oder Störung. Die drei Arten der Abweichung sind:
- Thrombozytopenie: Verminderte Konzentration der Blutplättchen im Blut mit Werten unter 150.000/µl. Unter 80.000/µl
ist mit einer erhöhten Blutungsneigung zu rechnen, unter 50.000/µl kann
es zu spontanen Blutungen (Nasenbluten, Blutergüsse) kommen. Konzentrationen unter 10.000/µl müssen bei medizinischer Notwendigkeit intensiv überwacht und gegebenenfalls
mit Thrombozyten-Konzentraten behandelt werden.
Ursachen können in einer verminderten Bildung, einem erhöhten Abbau oder Verbrauch liegen. Primäre, genetisch bedingte Ursachen einer Thrombozytopenie sind z. B. TAR-Syndrom, Wiskott-Aldrich-Syndrom, Jacobsen-Syndrom oder der Morbus Gaucher. Auch unter medikamentöser Therapie kann es gelegentlich zu einer Thrombozytopenie kommen, als sehr selten aber sehr gefährlich gilt dabei die durch Heparin oder andere niedermolekulare Heparine ausgelöste Heparin-induzierte Thrombozytopenie.
In der Schwangerschaft ist die Zahl der Thrombozyten im Blut häufig erniedrigt. Etwa 5–10 % der Schwangeren haben weniger als 150.000 Thrombozyten/µl.[4] Bei Werten unter 100.000/µl sollten andere Ursachen als die Schwangerschaft oder eine Schwangerschaftskomplikation in Betracht gezogen werden.[5]
- Thrombozytose: Erhöhte Konzentration der Blutplättchen im Blut mit Werten über 450.000/µl, die mit einem Risiko für
arterielle Thrombosen verbunden sein kann.
Eine primäre Ursache kann die Essentielle Thrombozythämie sein, eine Myeloproliferative Neoplasie.
Häufiger aber ist eine sekundäre Thrombozytose, auch „reaktiv“ genannt, etwa nach einer Milzentfernung (Splenektomie), bei bösartigen Tumoren oder chronisch-entzündlichen Erkrankungen (z. B. Morbus Crohn, rheumatische Erkrankungen), aber auch beispielsweise bei chronischem Eisenmangel oder nach akutem Blutverlust. Eine erhöhte Thrombozytenkonzentration kann auch ein allgemeiner Hinweis auf eine systemische Entzündung sein, assoziiert mit einer Aktivierung des proinflammatorischen Mediators Interleukin-6.
- Thrombozytopathie: Funktionsstörung der Blutplättchen ohne oder mit nur geringfügiger Veränderung der Konzentration
im Blut, die mit einer erhöhten Blutungsneigung einhergeht. Störungen betreffen die Funktion der Thrombozyten, also vor allem die Adhäsion und die Aggregation.
Die bekanntesten angeborenen Thrombozytenfunktionsstörungen sind die Glanzmann-Thrombasthenie, die mit einer mangelnden Aggregation der Thrombozyten einhergeht, sowie das Bernard-Soulier-Syndrom, eine Thrombozyten-Dystrophie mit Thrombozytopenie und erheblich vergrößerten Thrombozyten, „Riesenthrombozyten“, das sich durch eine Adhäsionsstörung auszeichnet.
Beim von-Willebrand-Syndrom liegt eine Koagulopathie vor mit einer Verminderung oder Funktionsstörung des Von-Willebrand-Faktors, wodurch die Thrombozytenadhäsion sekundär gestört ist und es zu einer gesteigerten Blutungsneigung kommt (auch Hämorrhagische Diathese genannt). Daneben sind aber die sekundären Thrombozytopathien durch exogene Ursachen viel häufiger, teilweise auch therapeutisch gewollt. Die Medikamentengruppe der Thrombozytenaggregationshemmer, zu denen z. B. Clopidogrel, und vor allem Acetylsalicylsäure zählt, wird sehr häufig zur Vorbeugung und Behandlung von Schlaganfällen, Herzinfarkten und anderen Durchblutungsstörungen eingesetzt. Aber auch bei Penicillin und Entzündungshemmern wie Diclofenac sowie bei einigen Chemotherapeutika in der Krebstherapie kann es zu einer Funktionsstörung kommen.
Geschichte
Thrombozyten wurden von Alfred Donné (1801–1878) wohl 1842 entdeckt[6] und 1844[7] zum ersten Mal als „Kügelchen“ im Blutplasma beschrieben.[8] 1865 beschrieb Max Schultze sie wesentlich genauer im Archiv für mikroscopische Anatomie,[9] erkannte sie jedoch nicht als eigene Zellart, sondern hielt sie für Abbauprodukte. Giulio Bizzozero korrigierte 1883 diesen Irrtum und erkannte auch als Erster die Funktion der Thrombozyten bei der Blutgerinnung.[10]
Wirtschaftliche Anwendung
Das Lysat aus (Spender-)Thrombozyten findet in der humanen Zellkultur als Nährmedienzusatz Anwendung (humanes Plättchenlysat).
Literatur
- R. Degkwitz: Studien über Blutplättchen in Folia Haematologica Leipzig 1920, XXV, S. 153
- D. B. Brewer: Max Schultze (1865), G. Bizzozero (1882) and the discovery of the platelet. In: Br J Haematol. 133(3), 2006 May, S. 251–258.
 PMID 16643426
PMID 16643426 - S2k-Leitlinie
 Thrombozytopathien der Gesellschaft für Thrombose- und
Hämostaseforschung (GTH). In: AWMF online (Stand: 15.07.2024)
Thrombozytopathien der Gesellschaft für Thrombose- und
Hämostaseforschung (GTH). In: AWMF online (Stand: 15.07.2024)
Einzelnachweise
- ↑ Wilhelm Gemoll: Griechisch-Deutsches Schul- und Handwörterbuch. München / Wien 1965.
- ↑ Jessica A. Reese, Jennifer D. Peck, David R. Deschamps, Jennifer J. McIntosh, Eric J. Knudtson, Deirdra R. Terrell,
Sara K. Vesely, James N. George: Platelet Counts during Pregnancy. In: New England Journal of Medicine, 2018, Band 379, Ausgabe 1 vom 5. Juli 2018, S. 32–43,
 doi:10.1056/NEJMoa1802897.
doi:10.1056/NEJMoa1802897.
- ↑ N. Mackman: Role of tissue factor in hemostasis and thrombosis. In: Blood Cells Mol Dis. 36(2), 2006 Mar-Apr, S. 104–107. Review.
- ↑ F Boehlen, P Hohlfeld, P Extermann, TV Perneger, P de Moerloose.: Platelet count at term regnancy: a reappraisal of the threshold. In: Obstet Gybecol. Band 95, Nr. 1, 2000, S. 29–33.
- ↑
 Platelet Counts during
Pregnancy. In: NEJM. (englisch).
Platelet Counts during
Pregnancy. In: NEJM. (englisch).
- ↑ Paul Diepgen, Heinz Goerke: Aschoff/Diepgen/Goerke: Kurze Übersichtstabelle zur Geschichte der Medizin. 7., neubearbeitete Auflage. Springer, Berlin/Göttingen/Heidelberg 1960, S. 36.
- ↑ Barbara I. Tshisuaka: Donné, Alfred. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 322.
- ↑ Alfred Donné: De l’órigine d. glob. du sang etc. In: Comptes rend. Soc. Biolog. 1844, t. XIV.
- ↑ M. Schultze: Ein heizbarer Objecttisch und seine Verwendung bei Untersuchungen des Blutes. In: Arch Mikrosc Anat. 1, 1865, S. 1–42.
- ↑ V. Gazzaniga, L. Ottini:
 The discovery of platelets and their function. (PDF) In: Vesalius, 7, 2001, (1),
S. 22–26.
The discovery of platelets and their function. (PDF) In: Vesalius, 7, 2001, (1),
S. 22–26.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 24.01. 2026