Butane
| Eigenschaften der Butane | ||
| Name | n-Butan | Isobutan |
| Strukturformel | 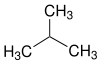 | |
| CAS-Nummer | 106-97-8 | 75-28-5 |
| PubChem | 7843 | 6360 |
| Summenformel | C4H10 | |
| Molare Masse | 58,12 g/mol | |
| Kurzbeschreibung | bei 20 °C und 1013 mbar gasförmig | |
| Schmelzpunkt | −138,29 °C | −159,42 °C |
| Siedepunkt | −0,50 °C | −11,7 °C |
| Dampfdruck (20 °C) | 208 kPa | 301,9 kPa |
| Dichte bei 0 °C, 1013 hPa | 2,71 kg/m3 | 2,70 kg/m3 |
| Löslichkeit in Wasser bei 20 °C | 61 mg/l | 49 mg/l |
| Untere
Explosionsgrenze (UEG) |
1,4 Vol% | 1,5 Vol% |
| 33 g/m3 | 37 g/m3 | |
| Obere
Explosionsgrenze (OEG) |
9,4 Vol% | 9,4 Vol% |
| 231 g/m3 | 231 g/m3 | |
Die Butane sind eine Stoffgruppe innerhalb der Alkane, die die Summenformel C4H10 aufweisen. Sie besteht aus den beiden Vertretern n-Butan und iso-Butan, die zueinander isomer sind. Beide Butane sind farblose, brennbare, leicht zu verflüssigende Gase („Flüssiggase“), die sich kaum in Wasser, aber gut in Ethanol und Ether lösen.
Vorkommen und Darstellung
Butane kommen natürlich im Erdgas vor, werden aber auch durch Cracken aus Erdöl gewonnen. Eine Trennung der beiden Isomere kann durch Adsorption und fraktionierte Desorption ab Aktivkohle oder Zeolithen erfolgen. Isobutan wird in großen Mengen aus n-Butan durch Isomerisierung mit einem Gemisch von Aluminiumchlorid und Chlorwasserstoff als Katalysator hergestellt.
Verwendung
Große Bedeutung haben die Butane als Brenngas (z.B. Feuerzeuggas), Kältemittel (Isobutan: R600a) sowie als Treibgase. Gasgemische aus z.B. 40 % Propan und 60 % Butan werden für technische Geräte wie Löt- und Schweißgeräte, Gas-Rechauds, Feuerzeuge usw. verwendet.

Im Winter wird Otto-Kraftstoff (Benzin) mit einem höheren Butangehalt verkauft als im Sommer, da Butan wegen des tiefen Siedepunktes die Kaltstartfreudigkeit des Otto-Motors bei tiefen Außentemperaturen verbessert.
Butane werden vielfältig in der chemischen Industrie zur Darstellung von C4-Alkenen wie 1,3-Butadien, 1-Buten, 2-Buten und Isobuten sowie für Synthesen höherer Kohlenwasserstoffe (für „Alkylatbenzin“), Thiophen sowie von Oxidationsprodukten wie tert-Butylhydroperoxid eingesetzt.
Sicherheitshinweise
Butane besitzen – wie alle Alkane – eine narkotische und sauerstoffverdrängende Wirkung. Bei einer dadurch ausgelösten Atemdepression können Effekte auf das Zentralnervensystem wie Erregung, Euphorie und Erbrechen, bei hohen Dosierungen auch negative Wirkungen auf Blutkreislauf und Herz (wie Herzrhythmusstörungen) auftreten.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 18.07. 2021